Биология клетки/Часть 1. Клетка как она есть/10/2
| Глава 10.2 | ||
| Деградация белков. Строение и работа протеасом | ||
Белки не вечны. Они вступают в химические реакции, в результате которых «портятся», утрачивают работоспособность. Поэтому практически все белки в клетке и в организме регулярно заменяются. «Испорченные» белки внутри клеток метятся с помощью специального белка — убиквитина. Помеченные убиквитином белки поступают в специальные органоиды — протеасомы, внутри которых распадаются на отдельные аминокислоты.


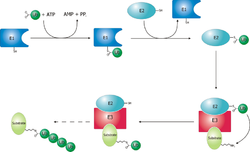
Убиквити́н (от англ. ubiquitous — вездесущий) — небольшой консервативный белок, который у эукариот может присоединяться к другим белкам. Убиквитинирование — это посттрасляционное присоединение ферментами убиквитин-лигазами одного или, чаще, нескольких мономеров убиквитина с помощью ковалентной связи к боковым аминогруппам белка-мишени. Присоединение убиквитина влияет на внутриклеточную локализацию и функцию белков. Самым первым открытием роли убиквитина в клетке стало доказательство его участия в деградации белков. Белки, помеченных мультиубиквитиновыми цепями, расщепляются с помощью 26S- протеасомы. Однако впоследствии оказалось, что система убиквитина вовлечена и в такие важные процессы, как размножение и дифференцировка клеток, реакция на стресс и патогены, репарация ДНК.
В 2004 г Аарон Чехановер, Аврам Гершко и Ирвин Роуз были удостоены Нобелевской премии по химии «за открытие убиквитин-опосредованной деградации белка».
[1] Биомолекула.ru/ Вездесущий убиквитин
А теперь немного о самих протеасомах. Есть два вида протеасом: 26S протеасомы и 20S протеасомы. 20S протеасома входит в качестве протеолитического ядра (камеры , где происходит деградация белков) в состав 26S протеасомы. 20S протеасома представляет собой полый цилиндр длиной 15-17 нм и диаметром около 11-12 нм. Он образован четырьмя лежащими друг на друге кольцами, состоящими каждое из семи белковых субъединиц, причем внешние кольца состоят из субъединиц а-типа, а внутренние - из субъединиц b-типа. Канал внутри такого цилиндра образует три камеры: большую центральную и две меньшие по краям. В центральной камере происходит протеолиз - расщепление белков на аминокислоты, а боковые камеры, за счет гидрофобности участков субъединиц а-колец, не дают белкам случайно проникнуть в протеолитическую камеру и тем самым препятствует случайному разрушению рабочих белков. Также субъединицы а-колец отвечают за присоединение к протеасоме других молекулярных комплексов, регулирующих её работу.
Маркировку белков, направляемых в протеасомы, осуществляет система убиквитинирования
правитьУ млекопитающих до 90% клеточных белков (не только всех короткоживущих, но и большинства долгоживущих) подвергается гидролизу в полости протеасомы. Однако, прежде чем начнется этот процесс, она должна распознать объект протеолиза по какому-то признаку, ярлыку. Оказалось, маркировкой занимается специальная система ферментов (ее называют системой убиквитинирования). Маркером же служит цепочка не менее чем из четырех молекул белка убиквитина, состоящего из 76 аминокислотных остатков. Как образование цепочки через остаток лизина-48 в каждой молекуле, так и присоединение ее к белку-субстрату как раз и обслуживается системой ферментов. Эта система, включающая три типа ферментов (Е1, Е2 и Е3), высоко специфична и избирательна за счет того, что построена по принципу иерархического усложнения. Фермент Е1 (в клетке он только один) активирует молекулу убиквитина и передает ее одному из ферментов семейства Е2 (их называют конъюгирующими). Затем в каскад реакций вступает третий участник — представитель семейства Е3, лигаз, “сшивающих” ферментов. Он принимает убиквитин от Е2, соединяется с белком-субстратом и ковалентно пришивает к нему цепочку убиквитина. Если Е1 не имеет разновидностей, то семейство Е2 насчитывает 13 членов в клетке дрожжей Saccharomyces cerevisiae, а у млекопитающих — гораздо больше. В семействе Е3 сейчас известно около 100 разных лигаз, они-то и определяют в конечном счете высокую специфичность всей протеолитической системы.
Почему же цепочка убиквитина пришивается именно к тому белку, чья судьба предрешена? Оказывается, он уже несет признаки смерти — специфические сигналы, которые включают процесс деградации. Ими могут быть участки внутри белковой молекулы или на ее N-конце. Видимо, в определенных условиях они становятся доступными для узнавания ферментной системой, ответственной за маркировку. К основным сигналам для присоединения убиквитина могут быть отнесены следующие: • конформация N-терминальной области пептида, в частности наличие «дестабилизирующей» N-концевой или другой свободной -аминогруппы («N-концевое правило») или специфически расположенный лизин субстрата; • определенные короткие мотивы в последовательности аминокислотных остатков • нарушения вторичной и третичной структуры белка (неправильное свертывание полипептидной цепи); • повреждение боковых цепей остатков аминокислот, в том числе их окисление (например окисление остатков метионина); • избыточное гликозилирование белков и пептидов.
Некоторые N-концевые аминокислотные остатки (у эвкариот особенно часто Арг, Лиз, Лей, Фен, Асп) играют большую роль в определении жизни многих короткоживущих белков (в среднем они существуют от нескольких минут до трех часов), а также частично разрушенных белков или белков с измененной третичной структурой. В ряде случаев дестабилизирующие аминокислоты присоединяются к N-концу долгоживущих белков специфическими ферментами, после чего такие белки быстро разрушаются протеасомой.
На зависимость скорости деградации от природы N-концевых аминокислот (правило N-конца) первым обратил внимание наш бывший соотечественник А.Варшавский, он же ввел понятие “короткоживущие белки”.
Цепочка убиквитина способна присоединяться к белку-мишени и по сигналам, возникающим за счет некоторых вторичных модификаций (например, фосфорилирования) или соединения со вспомогательными белками.
Протеасома расщепляет белки на короткие пептиды,попадающие в цитоплазму
правитьМаркировка белка-субстрата (мишени) цепочкой убиквитина завершилась. Теперь ее узнает и связывается с ней одна или более субъединиц регулятора РА700. Этот процесс, как и последующее разворачивание субстрата, нуждается в энергии АТФ. Видимо, роль АТФазы выполняет тот же белок-регулятор. Развернутая, линейная молекула белка протягивается через регулятор, играющий роль рта протеасомы, и через открытое отверстие в a-кольце проникает в протеолитическую камеру. Здесь белок расщепляется на полипептиды длиной от 5 до 24 аминокислотных остатков. Они высвобождаются из протеасомы и в цитоплазме могут подвергнуться гидролизу до аминокислот протеазами (например, эндопептидазами). Часть этих полипептидов переносятся в лизосомы и затем перемещаются на поверхность клетки в комплексе с белками МНС, определяя ее антигенные свойства. Ненужная больше маркировочная цепочка из молекул убиквитина ликвидируется: изопептидазы разрывают ее на мономеры.
Работа протеасом играет важную роль в регуляции жизнедеятельности клетки
правитьРасщепление белков в протеасомах – главный механизм регуляции времени жизни короткоживущих белков. Видимо, протеасомы принимают участие и в процессах деградации белков и пептидов с аномальной структурой. Деградация короткоживущих регуляторных белков через убиквитин-протеасомный путь играет важную роль в основополагающих процессах жизнедеятельности клетки. К таким белкам, например, относятся циклины, циклин-зависимые киназы и их ингибитры, супрессоры опухолей, онкобелки, активаторы транскрипции и их ингибиторы и многие другие. Весьма детально изучена деградация циклинов – регуляторных белков, которые синтезируются и затем быстро разрушаются на различных фазах клеточного цикла, контролируя тем самым его прогрессию.
Итак, деградация белка в протеасомах:
- регулирует время жизни важнейших белков,
- удаляет из клетки чужеродные и аномальные белки,
- поставляет образовавшиеся в результате гидролиза полипептиды в качестве антигенов, способных сообщать иммунной системе о неполадках в клетке.
Таким образом, внутриклеточный протеолиз — это не механический процесс деградации белков, а один из основных факторов, которые регулируют жизнедеятельность клетки.